記者 尾尻和紀 報道
キメラ抗原受容体T細胞免疫療法(Chimeric AntigenReceptor T-Cell Immunotherapy、略称CAR-T)は、新しいタイプの精密標的治療であり、治療の可能性を秘めています。がんに対する新規腫瘍免疫療法は、近年の臨床がん治療において非常に成功しており、急性リンパ芽球性白血病(ALL)およびさまざまな非ホジキンリンパ腫のサブタイプの患者における奏効率は80~90%と高いです。しかしながら、いくつかの固形腫瘍(例えば、神経芽腫、中皮腫、または膠芽腫)における効果は非常に限定的であり、臨床試験では、ほとんどのCAR-T細胞は数日から数週間で機能不全に陥り、これらの知見は腫瘍の微小環境が損なわれていることを示唆しています。
固形腫瘍はアルギニンを分解することでその増殖を促進し、その結果として生じる低アルギニン微小環境もまた、アルギニン再合成酵素であるアルギニノスクシネート合成酵素(ASS)およびオルニチンカルバモイル転移酵素(OTC)の発現が低いために、CAR-T細胞の増殖を阻害し、固形悪性腫瘍の臨床試験での有効性を制限しています。
このほど、バーミンガム大学の研究チームが、権威ある雑誌「Blood」に発表した論文「Metabolic engineering against the arginine microenvironment enhances CAR-T cell proliferation and therapeutic activity」を介して、機能的なASSまたはOTCを発現させたT細胞の再構成は、CAR-T細胞を欠損させることなくCAR-T細胞の増殖を促進するといいます。インビボでは、酵素修飾されたCAR-T細胞は白血病の有効性と固形腫瘍をクリアする能力を高め、CAR-T細胞を強化する機会を提供しています。この治療法は、第1の代謝制御戦略を提供します。

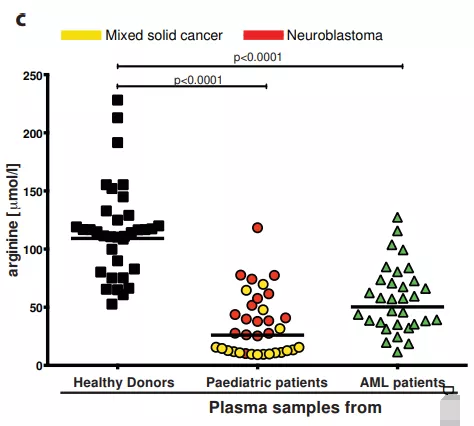
低アルギニン微小環境がT細胞増殖やCAR-T細胞応答を抑制する、AMLにおける末梢血アルギニン、神経芽腫 T細胞は細胞外アルギニン濃度に非常に敏感であるが、そのアルギニン再合成経路酵素は健康な対照細胞ほど敏感ではないため、細胞外アルギニン濃度には非常に敏感である。アルギニノスクシネート合成酵素(ASS)とオルニチン・トランスアミナーゼ(OTC)の発現は低いでした。
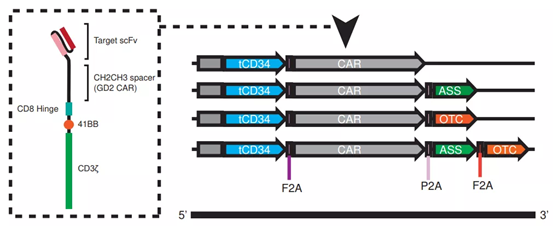
低アルギニン微小環境において、ASSおよび/またはOTCの挿入は、CAR-T細胞が再び自己を「燃料化」することを可能にします。著者らは、4つの共通の標的(抗GD2、-CD33、メソセリンおよび-EGFRvIII)に対して、ASS、OTC、またはその両方の酵素を共発現させるためのCAR-41BB-3ζ発現カセットを含むレトロウイルスベクターを再構成しました。
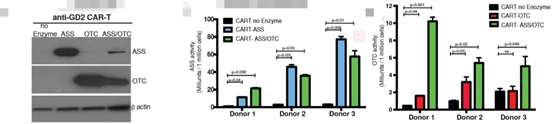
CAR-T細胞を増殖させ、高純度に選別し、絶望的なマウスに注入して腫瘍環境を模倣しました。ASSおよびOTC修飾されたCAR-T細胞は、GD2-CAR-T対照と比較して有意に増殖しました。低アルギニン腫瘍細胞調整培地でも同様の所見が観察されました。
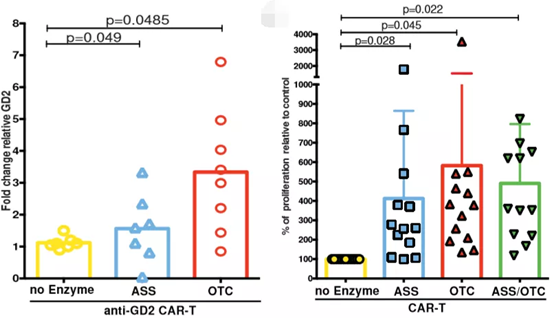

ASS修飾されたCAR-T細胞は、AMLを再刺激すると、白血病マウスの脾臓で有意な末梢拡大とそれに伴うAMLの減少を示しました。
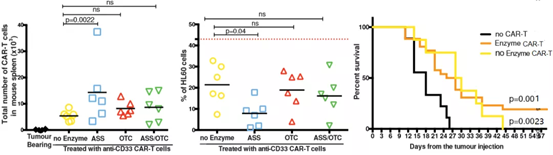
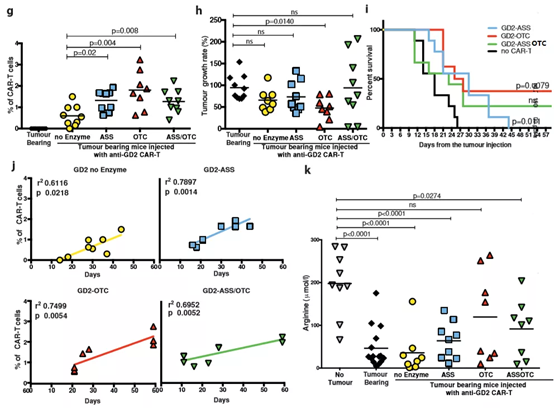
抗GD2 CAR-T細胞でGD2+ rhodomaマウスを処置すると、全生存期間および末梢血中の酵素が有意に改善されました。OTC-CAR-T細胞は腫瘍増殖率とマウスの生存率を大幅に低下させます。変更されたCAR-T増殖はマウスの生存と相関し、血漿アルギニンレベルを正常化します。
記者 尾尻和紀 報道