イノビオ社は2020年5月14日、新たに診断されたGBM(膠芽腫)を対象としたDNA製剤「INO-5401」と再生型メタPD-1抗体「Cemiplimab」との併用による第1/2相臨床試験の更新データをASCO会議で発表すると発表した。この治療により、GBMの1年生存率は85%(44/52)と劇的に改善し、GBMの治療スタンダードとなることが期待されています。

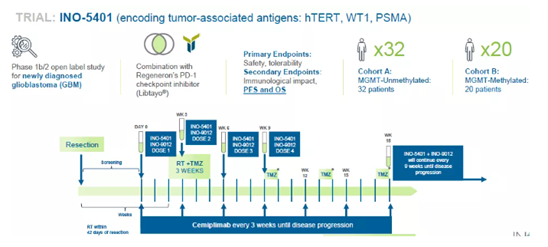
本試験は第1b/2相臨床試験で、2つのコホートに分けられ、新たにGBMと診断された52人の患者が登録されました。DNA製剤INO-5401とINO-9012を4回投与し、3週間ごとにCemiplimabを投与しました。主要評価項目は安全性と忍容性、副次評価項目はPFSとOSとしました。
イノビオ社のDNAドラッグ技術はユニークで、数々の重要な進歩を遂げてきました。
イノビオのDNAドラッグ技術は、電気パルスを介してDNAプラスミドを細胞内に転送する独自の送達装置CELLECTRAにも反映されています。
細胞内に入ったプラスミドは、特異的な抗原を発現し、この抗原を細胞に送達してT細胞応答を刺激し、一方でB細胞を刺激して治療目的の特異的な抗体を産生します。
INO-5041はWT1、PSMA、HTERTの3つの腫瘍抗原をコードし、INO-9012はIL-12をコードし、T細胞をさらに活性化します。2019年11月に開示されたデータによると、2つの治療サブグループの無増悪率は、標準治療ではそれぞれ40%から75%、60%から80%に上昇しました。
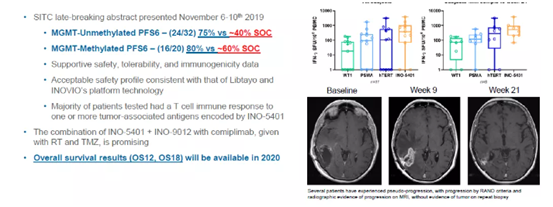
今回は1年生存率が85%と大幅に上昇し、18ヶ月の全生存率データが年内に公開される見込みです。
記者 尾尻和紀 報道